Анодная защита от коррозии
Анодная электрохимическая защита менее распространена, чем катодная электрохимическая защита. Это обусловлено тем, что она применяется для конструкций и сооружений, которые изготавливаются из низколегированных нержавеющих, углеродистых сталей, железистых высоколегированных сплавов, титана, и других разнородных пассивирующихся (способных к самостоятельной защите от коррозии) металлов. Анодная защита может применяться в хорошо электропроводных коррозионных средах.
При использовании анодной защиты, потенциал защищаемого металла смещается в более положительную сторону до тех пор, пока не будет достигнуто пассивное устойчивое состояние системы. При этом, достоинством анодной электрохимической защиты является не только очень значительное замедление скорости коррозии конструкции, но также и тот факт, что в производимый продукт и окружающую среду не попадают продукты коррозии.
Существуют несколько способов применения анодной защиты: смещение потенциала в положительную сторону используя источник внешнего электрического тока или введение в коррозионную среду окислителей или элементов в сплав, повышающих эффективность катодного процесса на поверхности металла. Анодная защита с использованием окислителей по механизму защиты схожа с анодной поляризацией.
Анодная защита с использованием окислителей по механизму защиты схожа с анодной поляризацией.
При использовании пассивирующих ингибиторов с окисляющими свойствами, защищаемая поверхность переходит в пассивное состояние под воздействием возникающего тока. К таким ингибиторам относят бихроматы, нитраты и др. Однако их использование достаточно сильно загрязняет окружающую технологическую среду.
Реакция восстановления деполяризаторов, протекающая на катоде, при введении в сплав добавок, проходит с меньшим перенапряжением, чем на защищаемом металле. Введение таких добавок осуществляется, в основном, с помощью легирования благородными металлами.
При пропускании электрического тока через защищаемую конструкцию, происходит смещение её потенциала в положительную сторону.
Установка для анодной электрохимической антикоррозионной защиты состоит из источника внешнего тока, электрода сравнения, катода и самого защищаемого объекта.
Для того, чтобы узнать, имеется ли возможность применить анодную электрохимическую защиту для определенного объекта, снимают анодные поляризационные кривые, помогающие определить потенциал коррозии исследуемой конструкции в определенной коррозионной среде, область устойчивой пассивности и плотность тока в этой области.
При изготовления катодов используют малорастворимые металлы, к которым относят высоколегированные нержавеющие стали, тантал, никель, свинец, платину.
Для того, чтобы анодная электрохимическая защита в определенной среде была эффективной, возникает необходимость использования легкопассивируемых металлов и сплавов. При этом электрод сравнения и катод должны все время находится в растворе, а также соединительные элементы должны быть выполнены качественно. Для каждого индивидуального случая анодной защиты схема расположения катодов проектируется отдельно.
Чтобы анодная защита была эффективной для определенного объекта, необходимо, чтобы он отвечал следующим требованиям:
— все сварные швы должны быть выполнены качественно;
— материал, из которого выполнен защищаемый объект, в технологической среде должен переходить в пассивное состояние;
— количество щелей и воздушных карманов должно быть минимальным;
— на конструкции не должны присутствовать заклепочные соединения;
— в защищаемом устройстве электрод сравнения и катод должны всегда находиться в растворе.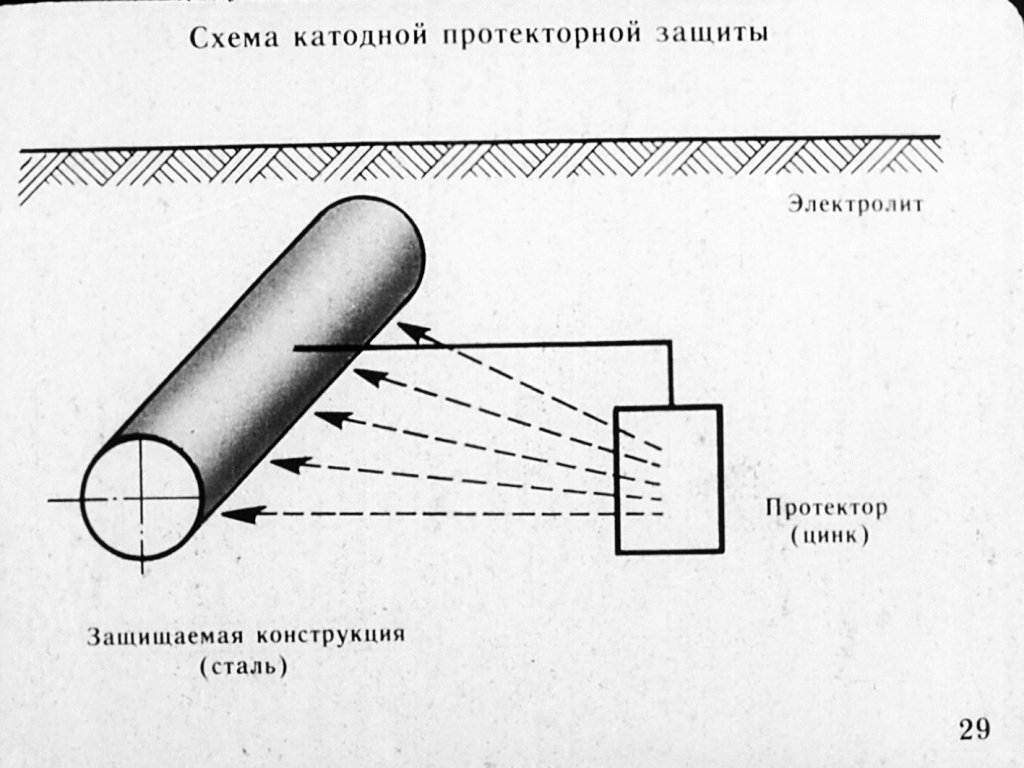
Часто для реализации анодной защиты в химической промышленности используют теплообменники и установки, которые имеют цилиндрическую форму.
Электрохимическая анодная защита нержавеющих сталей используется для производственных хранилищ серной кислоты, минеральных удобрений, растворов на основе аммиака, а также всевозможных цистерн, сборников, мерников.
Анодная защита также применяется для недопущения коррозионного разрушения ванн химического никелирования, теплообменных установок на производствах искусственного волокна и серной кислоты.
технология, виды и средства защиты труб и трубопроводов от коррозии
Содержание
- Электрохимическая защита
- Катодная защита
- Протекторная защита
- Анодная защита
- Электродренажная защита
Трубопроводные магистрали сегодня являются наиболее распространенным средством для осуществления доставки носителей энергии. К сожалению, у них есть существенный недостаток – они подвержены образованию ржавчины. Чтобы избежать появления коррозии на магистральных трубопроводах, выполняют катодную защиту. В чем же заключается ее принцип действия?
К сожалению, у них есть существенный недостаток – они подвержены образованию ржавчины. Чтобы избежать появления коррозии на магистральных трубопроводах, выполняют катодную защиту. В чем же заключается ее принцип действия?
В наши дни существует много способов защиты водопроводов от коррозии. Суть их проста: металл, из которого изготовлены трубы, вступает в реакцию с определенными растворами и веществами. Результатом процесса становится образование небольшой защитной пенки.
Специалистами выделяются следующие методы защиты трубопроводов от коррозии:
Электрохимическая защита
Достаточно результативный способ защиты металлоконструкций от электрохимической коррозии. Иногда воссоздать лакокрасочную оболочку или защитное оберточное покрытие просто невозможно. Вот в таких случаях и уместно применение электрохимической защиты.
Восстановление покрытия трубопровода, расположенного под землей, или днища морского судна – процесс достаточно трудоемкий и дорогой, а в некоторых случаях и невозможный.Благодаря электрохимической защите изделие будет надежно защищено от коррозии: покрытия подземных трубопроводов, днищ судов, всевозможных резервуаров не будут разрушаться.
- Используется метод в ситуациях, когда потенциал свободной коррозии пребывает в области усиленного распада основного металла или перепассивации. То есть, когда металлоконструкция интенсивно разрушается.
- При электрохимической защите к изделию из металла подключают постоянный электрический ток. Благодаря ему на поверхности металлической конструкции образуется катодная поляризация электродов микрогальванических пар и анодные области становятся катодными. А вследствие негативного влияния коррозии разрушается не металл, а анод.
- Электрохимическая защита может быть анодной или катодной: это будет зависеть от того, в какую сторону сдвинется потенциал металла (в положительную или в отрицательную).
Катодная защита
Метод, достаточно часто используемый для защиты металлоконструкций от коррозии. Применяется в тех случаях, когда металл не имеет склонности к пассивации. Суть метода проста: к изделию подается внешний электроток от отрицательного полюса, который обеспечивает поляризацию катодных участков коррозионных составляющих и поднимает значение потенциала до анодных. После прикрепления положительного полюса источника тока к аноду коррозия защищаемого изделия становится почти нулевой.
Применяется в тех случаях, когда металл не имеет склонности к пассивации. Суть метода проста: к изделию подается внешний электроток от отрицательного полюса, который обеспечивает поляризацию катодных участков коррозионных составляющих и поднимает значение потенциала до анодных. После прикрепления положительного полюса источника тока к аноду коррозия защищаемого изделия становится почти нулевой.
Анод требует периодической замены, так как со временем происходит его разрушение.
- Способы катодной защиты: поляризация от внешнего источника электротока, торможение развития катодного процесса, связь с металлом, имеющим более электроотрицательный потенциал свободной коррозии в определенной среде (протекторная защита).
-
С помощью поляризации от внешнего источника электротока защищают конструкции, находящиеся в почве и в воде, цинк, олово, алюминий и его сплавы, титан, медь и ее сплавы, свинец, высокохромистые, углеродистые, низколегированные и высоколегированные стали.

- Роль внешнего источника электротока выполняют станции катодной защиты. Их главные составляющие — выпрямитель, токоподвод к защищаемому объекту, анодные заземлители, электрод сравнения и анодный кабель.
- Катодная защита может быть использована в качестве самостоятельного или дополнительного способа коррозионной защиты.
Основной показатель результативности метода – защитный потенциал. Защитным называют тот потенциал, при котором быстрота коррозионного процесса металлического изделия становится минимальной.
Однако катодная защита обладает определенными недостатками. Один из них – опасность перезащиты. Такой эффект может наблюдаться в случае большого смещения потенциала защищаемого изделия в отрицательную сторону. Вследствие этого разрушаются защитные оболочки, начинается водородное охрупчивание металла, коррозионное растрескивание.
Протекторная защита
Вид катодной защиты, в процессе которого к защищаемому объекту подсоединяют металл с более высоким электроотрицательным потенциалом. При этом разрушается не металлоконструкция, а протектор. Через определенный промежуток времени протектор корродирует и его потребуется заменить на новый.
При этом разрушается не металлоконструкция, а протектор. Через определенный промежуток времени протектор корродирует и его потребуется заменить на новый.
- Эффект от протекторной защиты будет заметен только в том случае, если переходное сопротивление между протектором и окружающей средой незначительно.
- У каждого протектора есть свой радиус защитного действия – предельно возможное расстояние, на которое можно удалить протектор без утраты защитного эффекта. Протекторную защиту применяют, когда ток к объекту подвести трудно, дорого или просто невозможно.
- С помощью протекторов защищают объекты, находящиеся в нейтральных средах (море, реке, воздухе, почве и т.д.).
-
Материалом для изготовления протекторов служит магний, цинк, железо, алюминий. Металлы в чистом виде не смогут стать эффективной защитой для конструкций, поэтому, изготавливая протекторы, их дополнительно легируют.

Для изготовления железных протекторов используют углеродистые стали или чистое железо.
Анодная защита
Используется для титановых конструкций, объектов из низколегированных нержавеющих, углеродистых сталей, железистых высоколегированных сплавов, разнородных пассивирующихся металлов. Метод применяют в хорошо электропроводной коррозионной среде.
При анодной защите происходит сдвиг потенциала защищаемого металла в более положительную сторону. Смещение будет длиться до тех пор, пока не достигнется инертное устойчивое состояние системы. К преимуществам анодной электрохимической защиты можно отнести не только существенное торможение скорости коррозии, но и то, что продукты коррозии не оказываются в производимом продукте и среде.
-
Существует несколько способов реализации анодной защиты: можно сдвинуть потенциал в положительную сторону с помощью источника внешнего электротока или ввести в коррозионную среду окислители, которые способны повысить эффективность катодного процесса на металлической поверхности.

- Анодная защита с применением окислителей по защитному механизму имеет много общего с анодной поляризацией.
- При использовании пассивирующих ингибиторов с окисляющими характеристиками (бихроматов, нитратов и т.д.), защищаемая металлическая поверхность под воздействием возникшего тока становится пассивной. Однако эти вещества способны сильно загрязнять технологическую среду.
- Если ввести в сплав добавки, реакция восстановления деполяризаторов, которая происходит на катоде, пройдет не с таким большим перенапряжением, как на защищаемом металле.
- При прохождении электротока через защищаемую конструкцию потенциал сдвигается в положительную сторону.
- В состав установки для анодной электрохимической защиты входит источник внешнего электротока, электрод сравнения, катод и защищаемая конструкция.
Для эффективности метода в той или иной среде используют легкопассивируемые металлы и сплавы.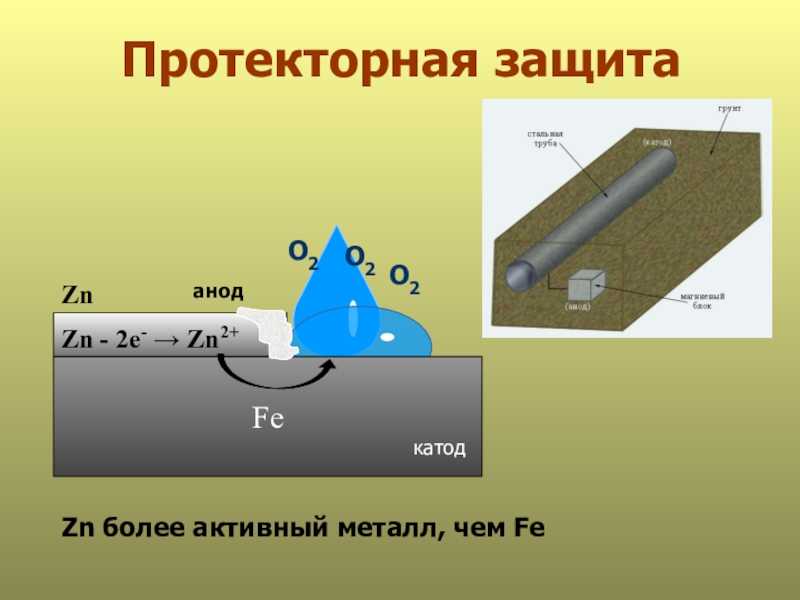
Подход к проектированию схемы расположения катодов должен быть индивидуальным для каждого случая.
Электрохимическую анодную защиту нержавеющих сталей используют для хранилищ серной кислоты, аммиачных растворов, минеральных удобрений, различных сборников, цистерн, мерников.
Анодную защиту используют, чтобы предотвратить коррозию ванн химического никелирования и теплообменных установок в изготовлении искусственного волокна и серной кислоты.
Электродренажная защита
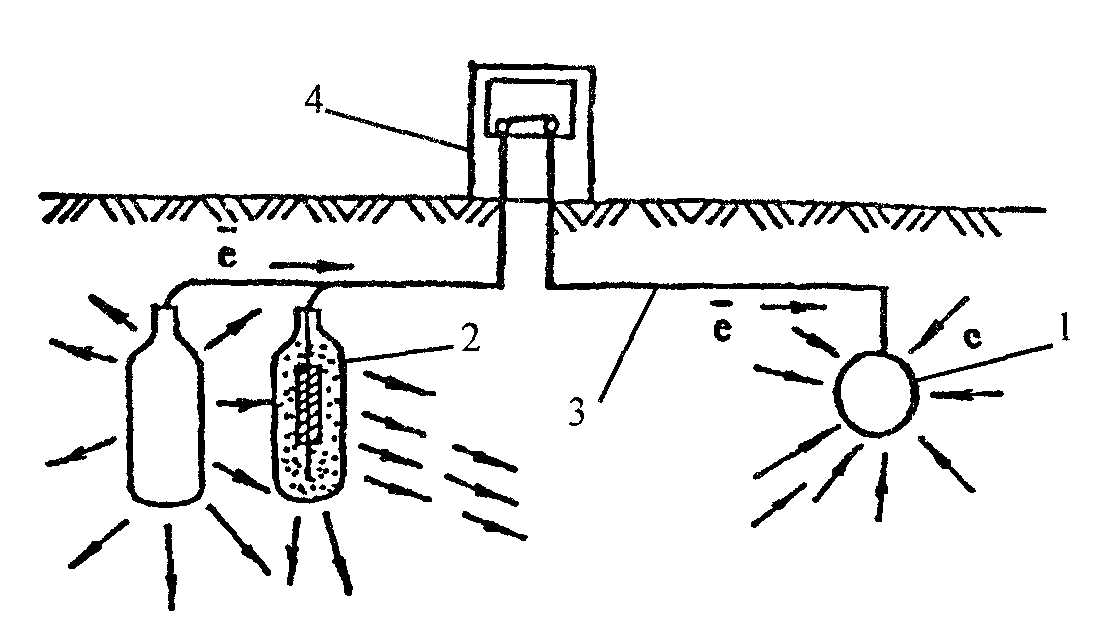
Это способ защиты трубопроводов от разрушения с помощью блуждающих токов. Метод предусматривает их дренаж (отвод) с защищаемой конструкции на источник блуждающих токов или специальное заземление.
-
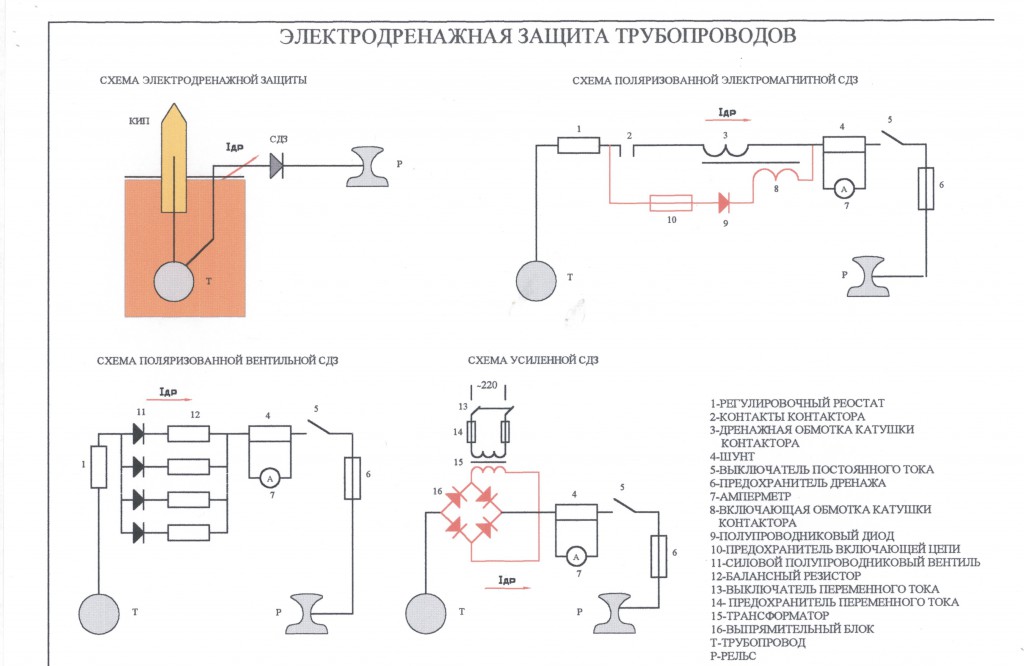
Дренаж бывает прямым, поляризованным и усиленным.
 Прямой электрический дренаж — это дренажное устройство, имеющее двустороннюю проводимость. При величине тока, превышающей допустимую величину, выйдет из строя плавкий предохранитель. Электрический ток пойдет по обмотке реле, оно включится, после чего произойдет включение звука или света.
Прямой электрический дренаж — это дренажное устройство, имеющее двустороннюю проводимость. При величине тока, превышающей допустимую величину, выйдет из строя плавкий предохранитель. Электрический ток пойдет по обмотке реле, оно включится, после чего произойдет включение звука или света. - Прямой электрический дренаж используют для тех трубопроводов, чей потенциал всегда выше потенциала рельсовой сети, служащей для отвода блуждающих токов. Иначе отвод станет каналом для натекания блуждающих токов на трубопровод.
- Поляризованный электрический дренаж является дренажным устройством, имеющим одностороннюю проходимость. Отличие поляризованного дренажа от прямого заключается в присутствии у первого элемента односторонней проводимости ВЭ. В случае поляризованного дренажа ток течет только в одном направлении — от трубопровода к рельсу. Это не позволяет блуждающим токам натекать на трубопровод по дренажному проводу.
-
Усиленный дренаж используется тогда, когда требуется не только отвести блуждающие токи с трубопровода, но и создать на нем определенную величину защитного потенциала.
 Усиленный дренаж – это обычная катодная станция. Ее отрицательный полюс подсоединяют к защищаемой конструкции, а положительный — к рельсам электрифицированного транспорта, а не к анодному заземлению.
Усиленный дренаж – это обычная катодная станция. Ее отрицательный полюс подсоединяют к защищаемой конструкции, а положительный — к рельсам электрифицированного транспорта, а не к анодному заземлению. - Как только трубопровод введут в эксплуатацию, регулируют работу системы его защиты от коррозии. Если возникает необходимость, осуществляют подключение станций катодной и дренажной защиты и протекторных установок.
Использование какой-либо из технологий защиты промысловых, стальных и прочих видов трубопроводов от коррозии – обязательная составляющая их эксплуатации. Все методы антикоррозийной защиты требуется реализовывать в строгом соответствии с ГОСТом.
Разница между анодной и катодной защитой
Основное различие между анодной и катодной защитой заключается в том, что при анодной защите защищаемая поверхность действует как анод, тогда как при катодной защите защищаемая поверхность действует как катод .
Анодная и катодная защита — это два электрохимических процесса, которые мы используем для предотвращения коррозии или ржавления поверхностей. В электрохимическом процессе мы используем электрохимическую ячейку с двумя электродами в качестве анода и катода. В процессах анодной и катодной защиты мы используем защищаемую поверхность (подложку) в качестве анода или катода, что приводит к названию этих процессов как таковых. Протекторная защита — это тип катодной защиты, при котором мы используем металл в качестве расходуемого анода. В этом процессе этот жертвенный металл подвергается коррозии, избегая коррозии катода.
СОДЕРЖАНИЕ
1. Обзор и основные отличия
2. Что такое анодная защита
3. Что такое катодная защита
4. Прямые сравнения – анодная и катодная защита в табличной форме
5. Резюме
Что такое анодная защита ?
Анодная защита — это тип электрохимического процесса, при котором мы можем защитить металлическую поверхность, сделав ее анодом в электрохимической ячейке. Мы можем обозначить это как AP. Однако этот метод возможен только для комбинаций материала и среды, которые показывают довольно широкие пассивные области. то есть сталь и нержавеющая сталь в 98% серная кислота.
Мы можем обозначить это как AP. Однако этот метод возможен только для комбинаций материала и среды, которые показывают довольно широкие пассивные области. то есть сталь и нержавеющая сталь в 98% серная кислота.
В АП нам нужно довести металл до высокого потенциала. Затем металл становится пассивным за счет образования защитного слоя. Однако AP не используется широко в качестве катодной защиты, поскольку он ограничен металлами, имеющими на поверхности достаточно надежный пассивный слой; например, нержавеющая сталь.
При применении AP необходимо учитывать два основных момента. Во-первых, нам нужно убедиться, что вся система находится в пассивном диапазоне. Во-вторых, нам необходимо иметь точное представление об ионах, что может привести к обширной точечной коррозии.
Что такое катодная защита?
Катодная защита — это тип электрохимического процесса, при котором мы можем защитить металлическую поверхность, сделав ее катодом в электрохимической ячейке. Мы можем обозначить его как CP.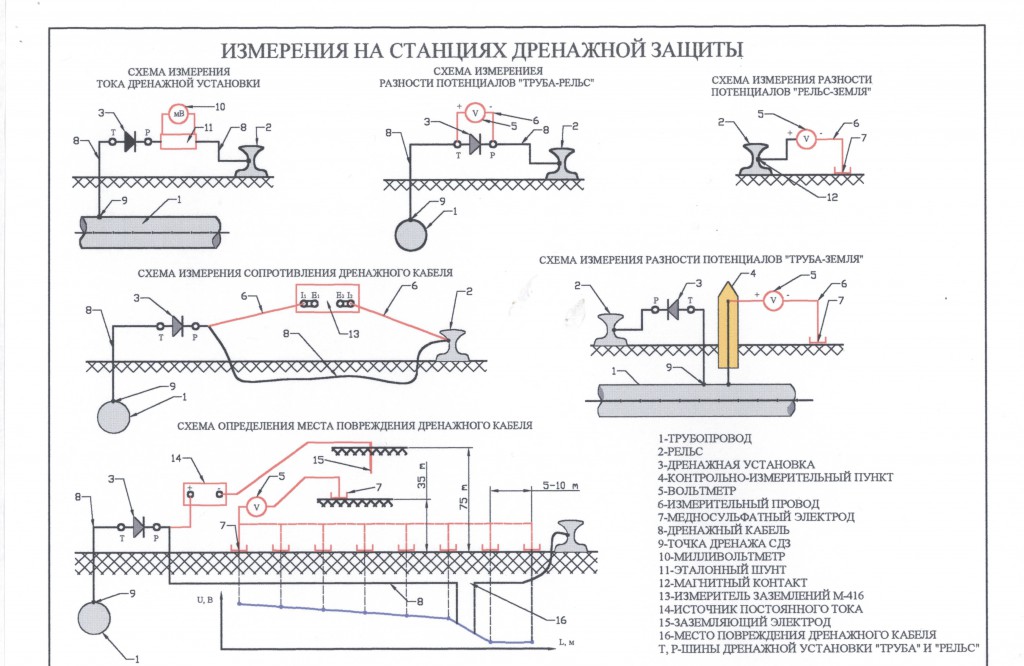 CP может предотвратить коррозию металлических поверхностей. Существуют различные типы CP; например, гальваническая защита или протекторная защита, системы импульсного тока и гибридные системы.
CP может предотвратить коррозию металлических поверхностей. Существуют различные типы CP; например, гальваническая защита или протекторная защита, системы импульсного тока и гибридные системы.
Рисунок 01: Системы подаваемого тока
В этом методе корродирует жертвенный металл, а не защищаемый. Если мы используем катодную защиту для больших конструкций, таких как длинные трубопроводы, метода гальванической защиты недостаточно. Следовательно, нам необходимо обеспечить достаточный ток, используя внешний источник питания постоянного тока.
Рисунок 02: Жертвенный анод – слой цинка
Кроме того, мы можем использовать эту технику для защиты топливных или водопроводных трубопроводов, изготовленных из стали, резервуаров для хранения, корпусов кораблей и лодок, оцинкованной стали и т. д.
Что такое Разница между анодной и катодной защитой?
Анодная защита — это тип электрохимического процесса, в котором мы можем защитить металлическую поверхность, сделав ее анодом в электрохимической ячейке, а катодная защита — это тип электрохимического процесса, в котором мы можем защитить металлическую поверхность, сделав ее катодом. в электрохимической ячейке. Таким образом, ключевое различие между анодной и катодной защитой заключается в том, что при анодной защите защищаемая поверхность действует как анод, тогда как при катодной защите она является катодом.
в электрохимической ячейке. Таким образом, ключевое различие между анодной и катодной защитой заключается в том, что при анодной защите защищаемая поверхность действует как анод, тогда как при катодной защите она является катодом.
Кроме того, анодная защита включает подавление реакционной способности металла путем регулирования потенциала более реакционноспособного металла; однако катодная защита включает изменение направления тока между двумя разнородными электродами. Следовательно, мы можем рассматривать и это как разницу между анодной и катодной защитой.
Резюме – Анодная и катодная защита
Анодная защита – это тип электрохимического процесса, в котором мы можем защитить металлическую поверхность, сделав ее анодом в электрохимической ячейке, а катодная защита – это тип электрохимического процесса, в котором мы может защитить металлическую поверхность, сделав ее катодом в электрохимической ячейке. Основное различие между анодной и катодной защитой заключается в том, что при анодной защите защищаемая поверхность действует как анод, тогда как при катодной защите она является катодом.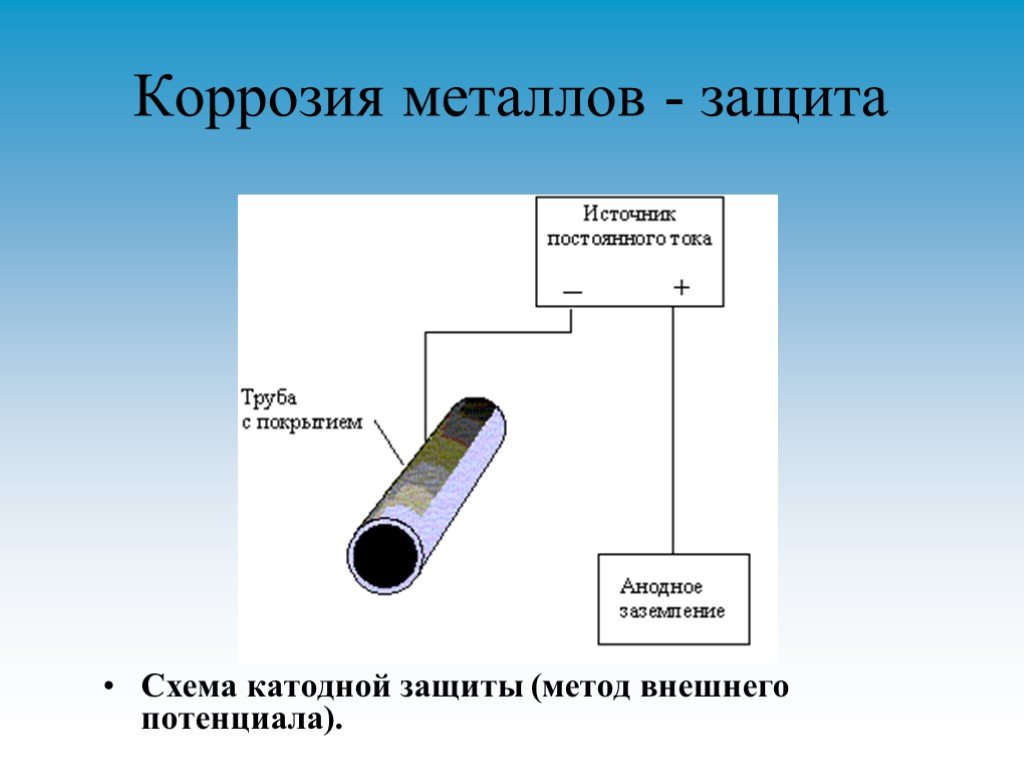
Ссылка:
1. «Что такое жертвенная защита? — Определение из Corrosionpedia». Corrosionpedia, доступно здесь.
Изображение предоставлено:
1. «Диаграмма катодной защиты» Кафе Нервоза — собственная работа (CC BY-SA 3.0) через Commons Wikimedia
2. «Жертвенный анод» Цвергельстерн (CC BY-SA 3.0) через Commons Wikimedia
Основы катодной защиты
Коррозия является естественным разрушительным явлением, которое возникает, когда некоторые металлы подвергаются воздействию окружающей среды. Реакция между воздухом, влагой и металлической подложкой вызывает специфические химические реакции, в результате которых металл превращается в более химически стабильную форму оксида, гидроксида или сульфида. В металлах на основе железа, таких как сталь, коррозия проявляется в виде оксидов железа III, также известных как ржавчина.
Реклама
Для возникновения электрохимической коррозии должны присутствовать три компонента: анод, катод и электролит. Анод и катод обычно соединены непрерывным электрическим путем, при этом оба погружены в один и тот же электролит. Во время этого процесса анод подвергается коррозии, а катод остается незатронутым.
Анод и катод обычно соединены непрерывным электрическим путем, при этом оба погружены в один и тот же электролит. Во время этого процесса анод подвергается коррозии, а катод остается незатронутым.
Реклама
Рисунок 1. Типичная электрохимическая ячейка, показывающая поток электронов от анода к катоду через электрическое соединение. (Источник: Alksub в английской Википедии / CC BY-SA)
Существуют различные методы предотвращения коррозии и борьбы с ней. Один из них известен как катодная защита (CP). Этот метод работает путем соединения металла, который нужно защитить, с более легко подверженным коррозии «жертвенным металлом». Этот жертвенный металл преимущественно подвергается коррозии (действуя как анод), в то время как рассматриваемый более ценный металлический объект (действуя как катод) остается защищенным. В этой статье мы объясним, как работает этот метод жертвенной защиты, и опишем его различные применения.
Понимание гальванической или биметаллической коррозии
Чтобы понять, как работает катодная защита, мы должны сначала понять основы биметаллической коррозии, также известной как гальваническая коррозия. Биметаллическая коррозия, как следует из ее названия, представляет собой уникальный тип коррозии, возникающий при соединении двух металлов. Эта коррозия наблюдается в нескольких ситуациях, когда разнородные металлы находятся в прямом или косвенном контакте друг с другом. Биметаллическая коррозия обычно характеризуется ускоренной коррозией одного металла, в то время как другой остается незатронутым. Другими словами, один металл жертвует собой, защищая другой. (Более подробно этот процесс рассмотрен в статье «Почему два разнородных металла вызывают коррозию?»)
Коррозия в электрохимическом элементе обусловлена главным образом свойством, известным как разность потенциалов. Эта разность потенциалов заставляет электроны течь от одного металла в ячейке (анод) к другому металлу (катод), генерируя при этом небольшое количество электричества. По мере того, как электроны вытекают из анода, происходит окисление, вызывающее разрушение или коррозию анодного металла. Между тем, когда электроны текут к катоду, происходит восстановление, дополнительно защищающее катодный металл.
По мере того, как электроны вытекают из анода, происходит окисление, вызывающее разрушение или коррозию анодного металла. Между тем, когда электроны текут к катоду, происходит восстановление, дополнительно защищающее катодный металл.
Реклама
При биметаллической коррозии эта разность потенциалов является прямым результатом разности электродных потенциалов между двумя разнородными металлами. Когда металл погружается в электролит, он принимает электродный потенциал, который отражает способность металла окисляться или восстанавливаться. Электродный потенциал различных металлов отображается в виде списка, известного как гальванический ряд. (Дополнительную информацию см. в разделе «Введение в серию гальваники: гальваническая совместимость и коррозия».) Металлы, расположенные выше в таблице, считаются анодными (более электроотрицательными), а металлы, расположенные ниже в таблице, более катодными (более электроположительными). . Чем дальше друг от друга находятся контактирующие металлы в гальваническом ряду, тем больше разность потенциалов между металлами и тем сильнее коррозия на аноде.
Катодная защита (CP) и метод ее работы
Несмотря на то, что конструкция систем катодной защиты может быть сложной, их действие основано на концепции биметаллической или гальванической коррозии, описанной ранее. Понимая принципы этого типа коррозии, мы можем намеренно соединять металлы вместе, чтобы гарантировать катодную защиту одного из них от другого. Другими словами, если мы хотим защитить определенную металлическую конструкцию, мы можем создать условия, при которых этот металл станет катодом электрохимической ячейки. Электрически соединяя защищаемый металл с более анодным (электроотрицательным) металлом, мы можем гарантировать, что анод жертвует собой, корродируя преимущественно по сравнению с катодным аналогом.
В некоторых случаях внешние источники питания могут использоваться для подачи дополнительных электронов в электрохимический процесс, что может повысить эффективность катодной защиты.
Системы катодной защиты используются во многих отраслях промышленности для защиты широкого спектра конструкций в сложных или агрессивных средах. В частности, в нефтяной и газовой промышленности системы катодной защиты используются для предотвращения коррозии топливопроводов, стальных резервуаров для хранения, морских платформ и обсадных труб нефтяных скважин. В морской промышленности этот метод защиты также используется для стальных свай, пирсов, причалов и корпусов судов. Другой распространенный тип катодной защиты, известный как цинкование, обычно используется для защиты стальных элементов и конструкций. (Чтобы узнать больше, прочтите «Гальванизация и ее эффективность в предотвращении коррозии».)
В частности, в нефтяной и газовой промышленности системы катодной защиты используются для предотвращения коррозии топливопроводов, стальных резервуаров для хранения, морских платформ и обсадных труб нефтяных скважин. В морской промышленности этот метод защиты также используется для стальных свай, пирсов, причалов и корпусов судов. Другой распространенный тип катодной защиты, известный как цинкование, обычно используется для защиты стальных элементов и конструкций. (Чтобы узнать больше, прочтите «Гальванизация и ее эффективность в предотвращении коррозии».)
Типы катодной защиты (CP)
Как упоминалось ранее, катодная защита работает путем преднамеренного формирования гальванического элемента с другим жертвенным металлом. Это может быть достигнуто за счет использования двух различных типов катодной защиты: пассивной катодной защиты и катодной защиты подаваемого тока.
Пассивная катодная защита
В системах пассивной катодной защиты расходуемый анод прямо или косвенно соединен с защищаемым металлом.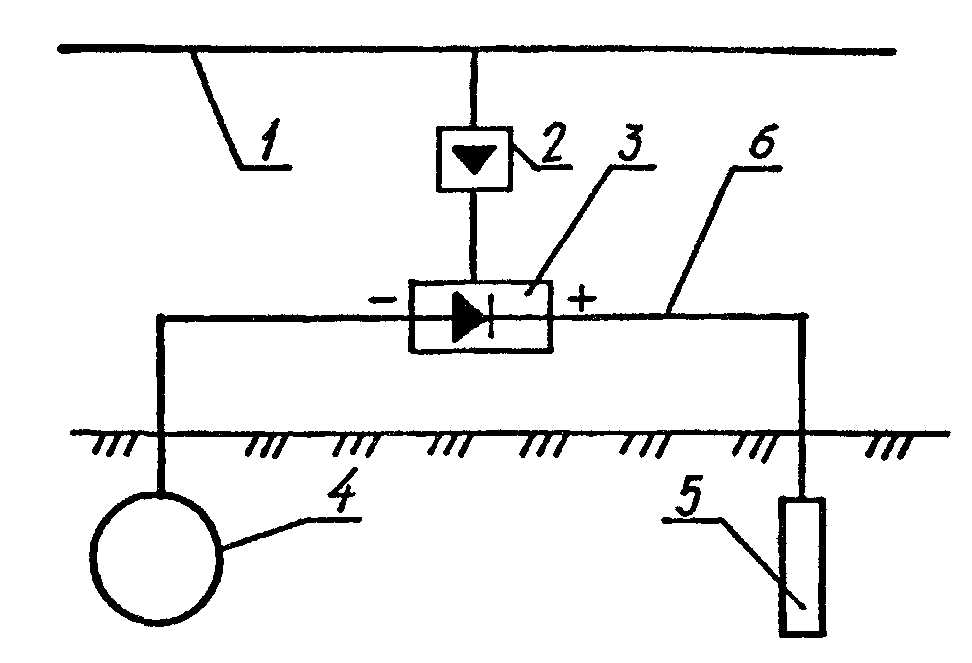 Разность потенциалов между двумя разнородными металлами генерирует достаточное количество электричества для формирования электрохимической ячейки и запуска гальванической или биметаллической коррозии.
Разность потенциалов между двумя разнородными металлами генерирует достаточное количество электричества для формирования электрохимической ячейки и запуска гальванической или биметаллической коррозии.
Этот тип защиты обычно используется в нефтегазовой промышленности для защиты стальных конструкций морских буровых установок и платформ. Здесь алюминиевые стержни (или другой подходящий металл) монтируются непосредственно на стальные секции, чтобы взять на себя роль жертвенного металла. Аналогичным методом катодно защищают стальные водонагреватели, резервуары и сваи.
Рисунок 2. Схема защиты трубопровода расходуемым анодом с использованием методов пассивной катодной защиты. Обратите внимание на отсутствие внешнего источника питания.
Другим распространенным примером пассивной катодной защиты является горячеоцинкованная сталь. Во время этого процесса стальные элементы или конструкции погружаются в ванну с расплавленным цинком, который покрывает объект. Когда сталь удаляется из расплавленного цинка, она вступает в реакцию с воздухом и влагой, образуя защитный слой, известный как карбонат цинка, который создает гальванический элемент со сталью.
Когда сталь удаляется из расплавленного цинка, она вступает в реакцию с воздухом и влагой, образуя защитный слой, известный как карбонат цинка, который создает гальванический элемент со сталью.
Когда стальной элемент поцарапан или поврежден, так что подложка обнажается, окружающее цинковое покрытие действует как расходуемый анод и подвергается коррозии преимущественно для защиты незащищенной стали. Этот тип защиты продолжается до тех пор, пока близлежащий цинк не истощится.
Катодная защита импульсным током (ICCP)
В крупных конструкциях использование методов пассивной катодной защиты может оказаться нецелесообразным. Количество расходуемых анодов, необходимых для подачи достаточного тока для обеспечения адекватной защиты, может быть либо нереалистичным, либо нецелесообразным. Чтобы решить эту проблему, используется внешний источник питания, который помогает управлять электрохимическими реакциями. Этот метод известен как катодная защита подаваемым током (ICCP). Системы ICCP идеально подходят для защиты протяженных сооружений, таких как подземные трубопроводы. Фланцы соединительных труб обычно изолируются с помощью изоляционных комплектов, чтобы разделить трубы на более мелкие и удобные секции в целях защиты ICCP.
Системы ICCP идеально подходят для защиты протяженных сооружений, таких как подземные трубопроводы. Фланцы соединительных труб обычно изолируются с помощью изоляционных комплектов, чтобы разделить трубы на более мелкие и удобные секции в целях защиты ICCP.
Рисунок 3. Схема объекта, защищенного анодом с использованием методов катодной защиты подаваемым током (ICCP). Обратите внимание, как задействован внешний источник питания постоянного тока.
Ограничения катодной защиты
В крупных трубопроводных сетях может быть много пересечений, параллелизма и подходов вблизи системы КП трубопровода. Между трубопроводами могут возникать помехи постоянного тока, что ускоряет коррозию. Чтобы решить эту проблему, трубопроводы могут быть электрически соединены либо напрямую, либо через сопротивление.
Для трубопроводов с покрытием катодное отслоение может произойти из-за высоких уровней CP, когда качество нанесенного покрытия низкое.

 Благодаря электрохимической защите изделие будет надежно защищено от коррозии: покрытия подземных трубопроводов, днищ судов, всевозможных резервуаров не будут разрушаться.
Благодаря электрохимической защите изделие будет надежно защищено от коррозии: покрытия подземных трубопроводов, днищ судов, всевозможных резервуаров не будут разрушаться.


 Прямой электрический дренаж — это дренажное устройство, имеющее двустороннюю проводимость. При величине тока, превышающей допустимую величину, выйдет из строя плавкий предохранитель. Электрический ток пойдет по обмотке реле, оно включится, после чего произойдет включение звука или света.
Прямой электрический дренаж — это дренажное устройство, имеющее двустороннюю проводимость. При величине тока, превышающей допустимую величину, выйдет из строя плавкий предохранитель. Электрический ток пойдет по обмотке реле, оно включится, после чего произойдет включение звука или света.  Усиленный дренаж – это обычная катодная станция. Ее отрицательный полюс подсоединяют к защищаемой конструкции, а положительный — к рельсам электрифицированного транспорта, а не к анодному заземлению.
Усиленный дренаж – это обычная катодная станция. Ее отрицательный полюс подсоединяют к защищаемой конструкции, а положительный — к рельсам электрифицированного транспорта, а не к анодному заземлению.